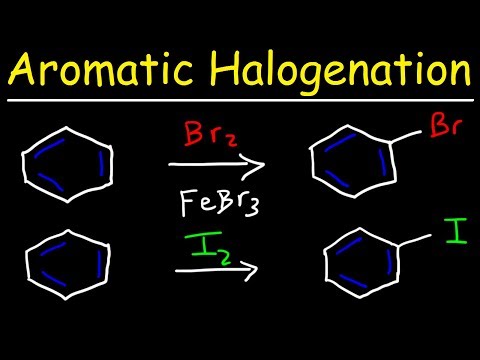
Når benzen omsættes med jod, er reaktionen reversibel i naturen. Det fører til dannelsen af reaktanter tilbage. Derfor oxiderer et oxidationsmiddel som HNO3 det HI, der dannes i reaktionen til I2, og holder reaktionen i fremadgående retning.
Hvorfor er jodering af benzen reversibel?
For iodering er reaktionen endotermisk med 12kJ/mol absorberet energi Derfor kan den ikke udføres ved hjælp af den konventionelle metode, der anvender Lewis-syrekatalysator og kræver stærke oxidationsmidler. Dette skyldes, at I2 føjer til benzenen, der reversibelt genererer HI.
Hvorfor udføres iodering af haloalkan ved hjælp af koncentreret HNO3?
Jodering af alkaner udføres i tilstedeværelse af oxidationsmidler, fordi et af produkterne er hydrogeniodid, som er et stærkt reduktionsmiddel, og det omdanner alkyliodid tilbage til en alkan.… Da reaktionen er reversibel i naturen, bruger vi oxidationsmidler som $HN{O_3}$ eller $HI{O_3}$ til at ødelægge HI.
Hvorfor er jodering af benzen svært?
Årsagen er: (i) I2 er den mindst reaktive af alle halogener, fordi den dannede C-I-binding er meget svagere end C-Cl- og C-Br-bindinger Jodbenzen dannet således tilbage til benzen. … Jodering kan også udføres i nærværelse af kviksølvoxid, som eliminerer HI som uopløseligt kviksølviodid.
Hvilken funktion tjener HNO3 i reaktionen mellem benzen og I2 for at producere jodbenzen?
Ved dannelsen af iodbenzen virker HNO3 som et reagens, der oxiderer jodmolekylet til iodkation (dvs. I+). Jodkationen fungerer som en elektrofil og gennemgår en elektrofil substitutionsreaktion for at danne iodbenzen.