Indholdsfortegnelse:
- Hvilke intermolekylære kræfter er til stede i eddikesyre?
- Hvilken intermolekylær kraft er s altsyre?
- Hvad er de intermolekylære kræfter i vand og eddikesyre?
- Er ethansyre dipol dipol?

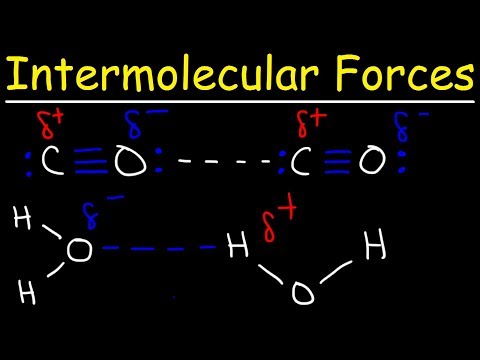
Video: Intermolekylære kræfter i chloreddikesyre?
2024 Forfatter: Fiona Howard | [email protected]. Sidst ændret: 2024-01-10 06:35
Chloreddikesyre, fordi London-dispersion tvinger London-dispersion fremtvinger London-dispersionskræfter (LDF, også kendt som dispersionskræfter, London-kræfter, øjeblikkelige dipol-inducerede dipolkræfter, Fluctuating Induced Dipole Bonds eller løst som van der Waals-kræfter) er en type kraft, der virker mellem atomer og molekyler, der norm alt er elektrisk symmetriske; det vil sige, at elektronerne er … https://en.wikipedia.org › wiki › London_dispersion_force
London dispersion force - Wikipedia
blandt dets molekyler er svagere. Chloreddikesyre, fordi dipol-dipolkræfterne blandt dens molekyler er svagere. Iodeddikesyre, fordi Londons dispersionskræfter blandt dens molekyler er stærkere.
Hvilke intermolekylære kræfter er til stede i eddikesyre?
I eddikesyre (med den kemiske formel $C{{H}_{3}}COOH$), har den tre typer intermolekylære kræfter, som er- hydrogenbinding, dipol-dipol-interaktioner og spredningskraft. Den har en særlig stærk type hydrogenbinding.
Hvilken intermolekylær kraft er s altsyre?
Der er to intermolekylære kræfter til stede i HCl: Dipol-dipol og London-dispersionskræfter. Af de to er dipol-dipolkræfterne stærkere. Dipol-dipolkræfterne stammer fra H-Cl-bindingsdipolen (da Cl er mere elektronegativ end H).
Hvad er de intermolekylære kræfter i vand og eddikesyre?
Vand har stærke hydrogenbindinger. Ligesom vand har eddikesyre stærke hydrogenbindinger. I fast eddikesyre danner molekylerne cykliske par forbundet med hydrogenbindinger.
Er ethansyre dipol dipol?
I eddikesyre (CH3COOH), hydrogenbinding, dipol-dipol-interaktioner og dispersionskraft er til stede, hvorimod i carbontetrachlorid (CCl4) kun upolære spredningskræfter er til stede.
Anbefalede:
Hvorfor er de intermolekylære kræfter dipoldipol?

Dipol-dipol-interaktioner: Disse kræfter opstår, når den delvist positivt ladede del af et molekyle interagerer med den delvist negativt ladede del af nabomolekylet. … Dipol-dipol-interaktioner er den stærkeste intermolekylære tiltrækningskraft .
Er dipole intermolekylære kræfter?

Dipol-dipol-interaktioner er en type intermolekylære attraktioner mellem to molekyler … En elektrisk monopol er en enkelt ladning, mens en dipol er to modsatrettede ladninger tæt på hver Andet. Molekyler, der indeholder dipoler, kaldes polære molekyler og er meget rigelige i naturen .
Intermolekylære kræfter i estere?

Estere, ligesom aldehyder og ketoner, er polære molekyler og har derfor dipol-dipol-interaktioner såvel som van der Waals-dispersionskræfter De danner dog ikke ester-ester-hydrogen bindinger, så deres kogepunkter er væsentligt lavere end for en syre med det samme antal kulstofatomer .
Hvorfor er chloreddikesyre surere?

Spørgsmål: Hvorfor er chloreddikesyre surere end eddikesyre? Svar: Kloreddikesyre er stærkere, fordi den indeholder (mere elektronegative) kloratomer i stedet for (mindre elektronegative) brintatomer . Hvorfor er chloreddikesyre surere end eddikesyre?
Intermolekylære kræfter i svovlbrinte?

H2S, H2Se og H2Te udviser dipol-dipol-intermolekylære kræfter, mens H2O udviser hydrogenbinding. I dette tilfælde er hydrogenbindingen af vand stærkere end dispersionen af H2Te . Har hydrogensulfid hydrogenbinding? Tænk for eksempel på hydrogensulfid, H2S, et molekyle, der har samme form som vand, men ikke indeholder hydrogenbindinger.






